1K
A diferença entre átomo e molécula é rapidamente explicada. Ambas as unidades são importantes para compreender o nosso mundo de um ponto de vista químico.
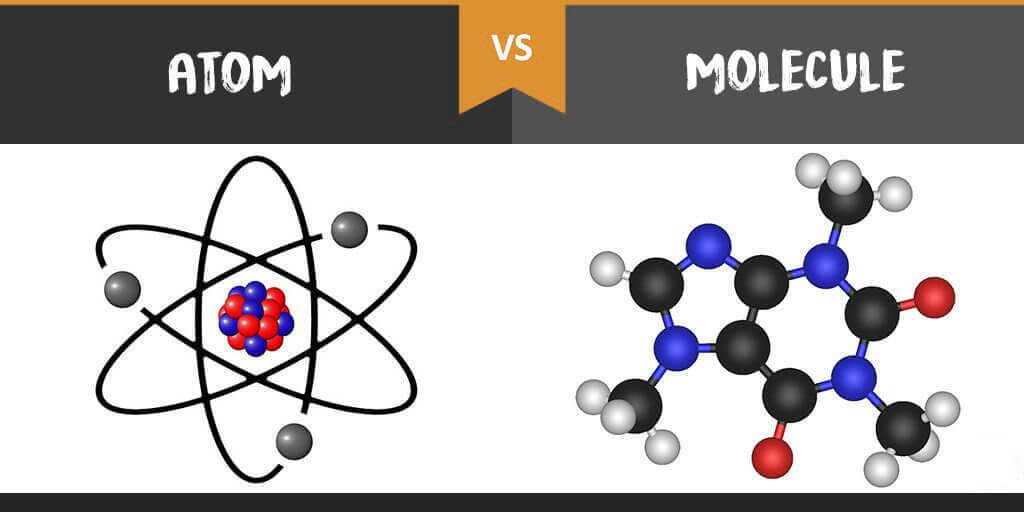
Diferença entre molécula e átomo explicada simplesmente
Unlike molecules, atoms are much smaller – because molecules are made of atoms. As moléculas são laços atómicos sólidos. Os átomos são a menor unidade em que a matéria pode ser dividida quimicamente ou mecanicamente.
- No entanto, os átomos também são constituídos por diferentes partículas, prótons, neutrões e electrões.
- Tudo o átomo tem um núcleo. É aqui que se encontram os prótons com carga positiva e os neutrões neutros.
- O núcleo é orbitado pelos electrões negativos. Eles movem-se em diferentes planos chamados shells.
É assim que se cria a ligação fixa
Os átomos têm diferentes números de conchas, dependendo do seu número de electrões. Um máximo de oito electrões cabem em cada concha. Os átomos – pode imaginar – são distribuídos do interior para o exterior das conchas.
- O mais exterior, a chamada concha de valência, não está, por isso, normalmente, totalmente ocupado. No entanto, para ter oito electrões na sua casca de valência, os átomos formam compostos. Chamamos então a estas moléculas.
- Compostos estáveis são formados quando os átomos são combinados para que cada átomo no composto tenha exactamente oito electrões de valência, mas alguns destes são partilhados com outros átomos.
- Um exemplo bem conhecido: Falta um átomo de oxigénio dois electrões na concha da valência. Por conseguinte, forma um composto com dois átomos de hidrogénio, cada um dos quais traz consigo um electrão. O composto é chamado H2O, mais conhecido como água.